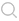【導讀】本文將詳解目前石墨烯在電化學過程中的理論計算結果,以超級電容器、鋰離子電池和ORR過程為典型代表,學習重要結論,加深對石墨烯功能的理解,也為新型石墨烯基電化學儲能器件提供研究思路。
石墨烯由于具有二維平面幾何特征和獨特的電子行為被廣泛用于電化學儲能研究領域,改善諸如超級電容器、鋰離子電池的輸出性能和提高氧還原過程(ORR)電催化活性。目前文獻中大量實驗結果報道也證實了石墨烯對不同儲能領域場合的作用。同時,研究者們也進行了大量的理論計算,從原子和電子的層次對石墨烯的作用機制進行解釋。
石墨烯電化學儲能的基本理論
從電化學角度來講,石墨烯在儲能器件中所起的作用主要有四種:一種是石墨烯不參與電化學反應,僅僅通過與電解液形成雙電層作用來存儲電荷,提高電容效果,這種情況主要出現(xiàn)在超級電容器中;另一種則是與活性物質發(fā)生電化學反應,通過電子轉移而產生法拉第電流,并為電化學反應的生成物提供存儲場所,如鋰離子電池等,或者雖然不發(fā)生電化學反應,但是可以通過與生成物相互作用而將其固定,同樣提供存儲場所,如鋰硫電池;同時,石墨烯還可以為電化學反應提供催化效果,降低電化學反應所需的能量勢壘,如ORR等;還有一種則是利用自身導電性提高電極的電導率,降低充放電過程中的歐姆電阻。本文主要圍繞前面三種作用展開。
石墨烯在儲能體系中的電化學行為與其電子結構息息相關。正確認識其電子結構將是更好利用石墨烯材料的有效前提,并且也可以為具體應用領域中石墨烯材料的電子結構調整提供指導思路。
石墨烯電子結構特征
1.石墨烯及其缺陷類型
石墨烯屬于由雙原子基點組成的三角布拉維點陣。由于相鄰的兩個碳原子位置不等同,石墨烯晶格可以分為兩個亞點陣,每個亞點陣都是三角布拉維格子。相鄰兩個C原子的間距為0. 142 nm,鍵角為120°,與分子苯中的數(shù)值相同。平面內部C 原子通過三個σ相互相連,在垂直平面上碳原子的pz軌道形成離域的π鍵。圖1給出了石墨烯的結構示意圖。
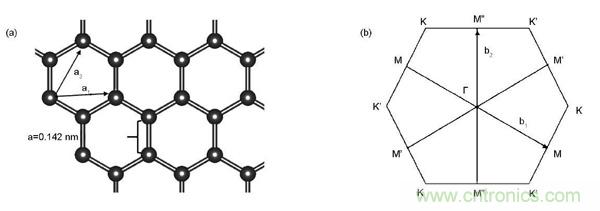
圖1.石墨烯的結構特征:(1)晶體結構;(2)布里淵區(qū)
布里淵區(qū)的三個高對稱點是Τ, K 和M, 分別是六邊形的中心、角和邊的中心,見圖1(2)。
石墨烯的能帶結構非常特殊,在倒易空間的K /K’處出現(xiàn)線性色散,即此處附近石墨烯電子能量線性變化,同時此處電子態(tài)密度為零。完整石墨烯的費米能級與Dirac點重合,在費米能級附近成鍵的π態(tài)和反鍵的π*態(tài)雙重簡并。
在石墨烯實際制備過程中,往往難以得到完整的石墨烯,總是存在各種缺陷。同時為了改善石墨烯的電子結構,賦予其不同的化學性能,研究者也會對石墨烯晶格進行調整,引入部分缺陷或異原子。石墨烯上常見的缺陷為Stone-Wales(SW)缺陷、單空位(V1)缺陷、雙空位(V2)缺陷和多原子缺陷,同時還會存在一維線形缺陷和晶界引起的缺陷等。
存在SW缺陷的石墨烯并沒有丟失C原子,只是將某個C—C鍵旋轉了90°,相鄰的四個六邊形變成兩個五邊形和兩個七邊形,所以此類缺陷也常稱為55-77缺陷。該缺陷的形成能非常高,缺陷位置相對固定。
當石墨烯失去一個C原子后,會出現(xiàn)一個空位,產生V1缺陷。由于C原子的缺失,石墨烯上會出現(xiàn)三個具有未飽和懸掛鍵的C原子,此時石墨烯發(fā)生Jahn-Teller形變,其中兩個C 原子相互靠近形成五邊形,只留下一個懸掛鍵。從而出現(xiàn)一個5元環(huán)和一個9元環(huán)。該缺陷的形成能也非常高,但是其遷移能壘較低,在較低溫度下就可以在石墨烯表面發(fā)生遷移。
當兩個相鄰的碳原子除去后,石墨烯上會出現(xiàn)V2缺陷。此時石墨烯上的4個6元環(huán)會變成兩個5元環(huán)和一個8元環(huán),即585-V2。該缺陷的形成能與單空位相當。
除了點缺陷之外,石墨烯內部還存在一維的線缺陷。一種是將不同取向的石墨烯微晶分開的晶界,通常由5元環(huán)、8元環(huán)組成。還有一種則是石墨烯的邊緣。由于具有懸掛鍵,邊緣結構式通常為armchair和zigzga取向。然而當這兩種邊緣有碳原子丟失時,邊緣的六元環(huán)中間會產生五元環(huán)和七元環(huán)。
2. 原子摻雜
N 原子經常引入到石墨烯內部來調控其電子結構。N摻雜石墨烯可以通過含N 前驅體對石墨烯或者氧化石墨烯后處理得到缺陷點的存在會減少N摻雜的形成能,所以N在缺陷石墨烯的摻雜比完整石墨烯容易,在N 摻雜之前有意引入缺陷會提高摻雜效果。對于完整石墨烯,由于N原子之間存在排斥力,N 原子摻雜位置分布比較分散,但是當存在缺陷時,由于缺陷與N之間的吸引力,缺陷附近區(qū)域N的分布將會非常集中。
B原子也經常引入石墨烯來調整其電子結構。由于B比C缺少一個電子,摻B之后石墨烯費米能級向低能級方向移動,與Dirac點不再重合。此外,S、P等原子也用來摻雜改進石墨烯的電子結構。
圖2給出了SW缺陷、V1和V2缺陷的具體結構。圖3為完整石墨烯、585-V2 石墨烯、SW缺陷石墨烯和石墨化N石墨烯的電子能帶圖。
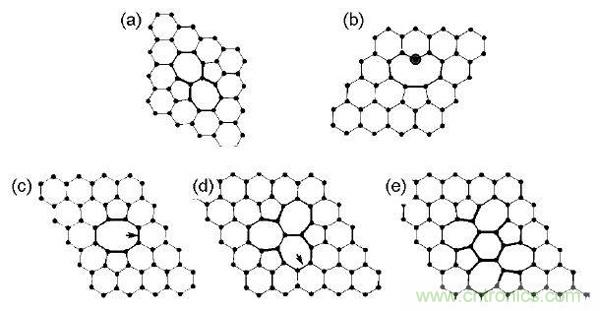
圖2.不同種類石墨烯缺陷:(a)S-W缺陷;(b)V1缺陷;(c)585-V2缺陷;(d) 555777-V2 缺陷;(e) 555-6-777-V2缺陷

圖3.不同類型石墨烯能帶結構:(a)完整石墨烯;(b)585-V2缺陷;(c)S-W缺陷;(d)N 石墨烯
下面根據(jù)石墨烯在儲能器件中所起的不同作用,分別從超級電容器、鋰離子電池和ORR過程對目前的理論研究進展進行討論。
超級電容器
完整的石墨烯量子電容非常小,在充電或放電過程中難以為電子提供足夠的能態(tài)來存儲電荷。為了提高石墨烯的量子電容,首先考慮到的是在石墨烯中引入缺陷結構,改善石墨烯在費米能級處的DOS。對于SW缺陷,由于費米能級處存在五元環(huán)和八元環(huán)碳原子上pz態(tài)組成的能帶,該能帶將會容納額外的電子,進而提高石墨烯可聚集的電量。同時,由于存在pz準局域態(tài),V2缺陷中缺陷附近的C原子也會容納額外的電子。SW缺陷在作為負極時存儲電荷非常有效,而V2缺陷則在作為正極時表現(xiàn)出良好的電荷存儲行為。晶格中C原子被N和B替換后都會對量子電容產生影響,前者對正偏壓范圍內量子電容提高,后者則是對負偏壓范圍內量子電容提高。
同時,科學家還詳細討論了石墨烯的層數(shù)、應力和表面褶皺等局部結構對量子電容的影響。由于單層石墨烯帶密度較低,難以有效屏蔽電極中產生的額外電荷,所以電壓容易隨電荷增加而迅速提高,電容效果較差。當石墨烯層數(shù)提高后,所能容納的電荷數(shù)提高,量子電容相應提高。
圖4為完整石墨烯、SW石墨烯、V1石墨烯、V2石墨烯、摻N石墨烯和摻B石墨烯量子電容的比較。當石墨烯在平面某個方向上尺度有限時會形成納米帶,此時電子結構特征與量子電容與完整石墨烯相比具有較大的變化。
過渡金屬原子也會對石墨烯的電子結構產生影響,并在石墨烯的空位上產生較強的吸附作用。

圖4.不同結構石墨烯量子電容:(a) 缺陷石墨烯;(b) N摻雜石墨烯;(c) N、B摻雜石墨烯
鋰離子電池
鋰離子電池的石墨烯理論研究主要集中在兩個方面,首先是容量問題,涉及到Li 與石墨烯的相互作用,再就是Li 離子在石墨烯上的擴散問題,這與鋰離子電池的倍率性能緊密相連,主要包括Li在石墨烯表面平行方向的擴散和穿過石墨烯表面的擴散。
1.容量與相互作用能
(1)完整石墨烯
Li 在完整石墨烯表面的相互作用研究表明,Li穩(wěn)定存在于石墨烯的C六元環(huán)中間,組成環(huán)的六個碳原子都與Li產生相互作用,而Li 在兩個碳原子的橋接位置和單個碳原子的頂端位置時的相互作用非常弱。Li與C六元環(huán)的相互作用具有離子鍵特征,電荷從Li向石墨烯轉移,遷移的電子主要集中在Li和C六元環(huán)之間的區(qū)域,所以Li原子上面區(qū)域和石墨烯上C-C鍵上的電子減少。當Li 吸附在石墨烯表面時,石墨烯的電子結構有了一定的變化。由于Li的電子進入石墨烯的π*帶,體系費米能級明顯上移,進入導帶,同時Li的2s態(tài)由于電荷轉移位于高于費米能級的位置,此時石墨烯仍然有Dirac點,但是由于電荷從Li轉移到了石墨烯,費米能級變得略高于狄拉克點。
科學家發(fā)現(xiàn),Li與石墨烯的吸附能大于0,表明Li與完整石墨烯不會自動發(fā)生吸附作用,難以形成穩(wěn)定化合物。而對于少層石墨烯,Li 則會與之自動發(fā)生反應。當Li進入少層石墨烯的層間時,Li與碳原子的相互作用受層間范德華力的影響,并且該影響隨著Li含量變化而變化。計算結果表明,少層石墨烯存儲Li的容量低于本體石墨。Li可以進入任何層數(shù)的少層石墨烯中,但是只能進入石墨烯層間,不能存在于少層石墨烯的表面。對于兩層石墨烯,當含量低時Li具有非常強的插層作用。當石墨烯層數(shù)繼續(xù)增加時,Li首先進入最外面的石墨烯層間,而不是中間的層間。隨后Li根據(jù)石墨烯層數(shù)的不同而具有不同的嵌入行為,或進入同樣的最外層間,或進入另一個最外層間或者進入內部層間。
另外,當采用Li在本體Li金屬的狀態(tài)作為參考態(tài),考察了Li在石墨烯上的吸附行為。采用該參考態(tài)時,Li在石墨烯表面的吸附能為負值,說明可以發(fā)生吸附,但是容量仍然低于石墨。石墨烯上不同Li原子之間存在庫倫排斥力,當Li的濃度很低時Li傾向于在石墨烯表面分散,故當濃度非常低時Li可以吸附在石墨烯上。但隨著Li增多,Li原子之間由于相互吸引會形成團簇而與石墨烯發(fā)生相分離,所以石墨烯的容量比石墨低。作者分析了Li團簇在石墨烯的吸附,發(fā)現(xiàn)吸附到石墨烯上團簇的內聚能高于孤立團簇的內聚能,表明前者更為穩(wěn)定。團聚進一步發(fā)展則會形成枝晶。
(2) 缺陷及雜化石墨烯
Li與帶有缺陷的石墨烯的相互作用與完整石墨烯具有較大的差異。Li與585的V2 缺陷石墨烯作用時,由于Li電子的轉移,V2石墨烯上費米能級附近原來近乎水平的能帶由于部分被電子占據(jù)而能量降低。然而,費米能級仍然在Dirac 點下方。Li與SW缺陷的石墨烯作用時,費米能級升高超過Dirac點而進入導帶,同時SW缺陷出現(xiàn)的那條近乎水平的能帶也部分被占據(jù)。
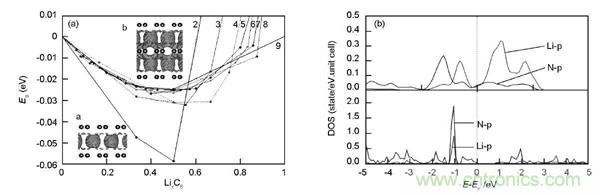
圖5.不同結構石墨烯與Li相互作用:(a)少層石墨烯; (b) Li與摻N石墨烯的態(tài)密度
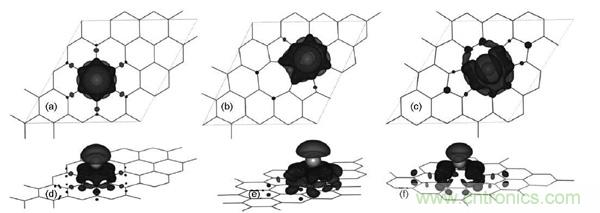
圖6.Li在缺陷石墨烯上電子差分密度圖:(a, d)完整石墨烯;(b, e) V1缺陷;(c,f)V2缺陷
2.擴散
在鋰離子電池系統(tǒng)中,石墨烯除能夠存儲Li之外,還有一個重要的考察因素是石墨烯對Li離子擴散過程的影響,這直接影響鋰離子電池的快速充放電行為。擴散過程包括兩方面,Li在石墨烯表面上并以與表面平行的方向進行擴散,另外一種是穿過石墨烯平面,以與平面垂直的方向擴散。
計算表明,Li在完整石墨烯表面的擴散勢壘是0. 32 eV,表明Li易沿著石墨烯表面擴散,利用石墨烯作為負極時往往具有良好的倍率性能??茖W家的計算結果表明,當Li在完整石墨烯上沿著六元環(huán)中心頂部—C—C鍵中間六元環(huán)中心頂部路徑擴散時,最高的能量阻礙在Li跨過C—C鍵的位置,能量勢壘為0. 311 eV;沿著六元環(huán)中心頂部—C原子頂部六元環(huán)中心頂部擴散時,C原子頂點為能量壁壘,0. 337 eV。當Li在兩層石墨烯的層間擴散時,同樣具有較低的擴散能壘。
石墨烯的缺陷對Li在平行石墨烯平面方向的擴散行為具有重要影響。Li在585結構的V2缺陷中擴散時,由于缺陷產生的能量陷阱,Li很容易被固定在缺陷區(qū)域。該缺陷上的擴散阻礙為0. 17 eV,而V1的擴散阻礙則是0. 24 eV,都小于完整石墨烯(0. 311 eV),所以該能量陷阱可以很大程度上減小Li的擴散勢能,進一步改善Li在石墨烯表面的擴散行為。
石墨烯內部經常出現(xiàn)晶界,尤其在通過CVD法制備的石墨烯中更是常見。晶界缺陷也會對石墨烯費米能級附近的電子態(tài)產生影響??茖W家對此進行研究,結果為Li在石墨烯上最穩(wěn)定的吸附位置在晶界上。以上缺陷結構對Li的吸附能力都優(yōu)于完整石墨烯。Li原子在石墨烯在平行和垂直晶界的擴散行為結果表明,Li原子在晶界上的平行擴散能壘明顯低于垂直晶界的擴散,說明Li原子很難橫向穿過晶界而到另外一個微晶區(qū)域。
Li在石墨烯片層垂直方向的擴散行為也對鋰離子電池的倍率性能產生重要的影響。Li透過完整石墨烯擴散時,由于庫倫排斥力,能量勢壘非常高,為9. 8 eV,所以Li難以通過六元環(huán)中心穿過完整石墨烯表面。當存在空位缺陷時,擴散阻礙降低??茖W家結合實驗和理論計算了Li在不同石墨烯上穿過時的能量勢壘,分別為完整石墨烯為10. 2eV,SW 缺陷位6. 35 eV,V1 為8. 86 eV,V2-585為2. 36 eV。所以從V2缺陷開始,Li基本可以透過石墨烯片層發(fā)生擴散。
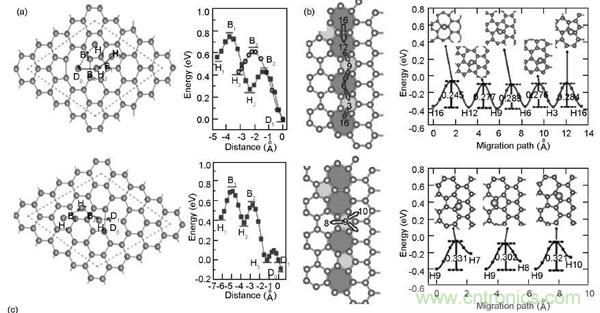
圖7.Li離子擴散過程:(a)平行石墨烯表面;(b)平行石墨烯晶界;(c)透過石墨烯平面
ORR過程
燃料電池可以直接將化學能轉變成電能,具有轉化效率高,功率密度高和無污染的優(yōu)點。O2還原反應是制約燃料電池發(fā)展的重要因素。該反應可以通過兩種路徑發(fā)生,第一是四電子過程,O2得到四個電子直接還原成H2O;第二是效率較低的兩電子過程,O2轉變?yōu)镠2O2。由于利用效率高,四電子過程的催化劑研究非常重要。
石墨烯催化效果計算表明,O2分子與完整石墨烯片層的吸附能都非常小,二者的距離也較大,大于2. 6 ?。雖然O2分子與石墨烯形成弱的離子鍵,但是由于反應過程中后續(xù)步驟所需能量非常高,并且生成的OOH也難以吸附在完整石墨烯上,所以完整的石墨烯沒有O2催化活性。由于N的電負性強于C,N周圍的C原子帶有正電荷,并且具有一定的自旋電荷。研究表明,當碳原子的自旋電荷密度或原子電荷密度高于0. 15時就會具有ORR的電化學活性。另外,科學家采用周期結構石墨烯模型詳細探討了完整石墨烯和摻N石墨烯上ORR過程,見圖8,同時還計算了N石墨烯上N含量對ORR過程的影響,發(fā)現(xiàn)4% ~5%的N含量對于應用是比較合適的。
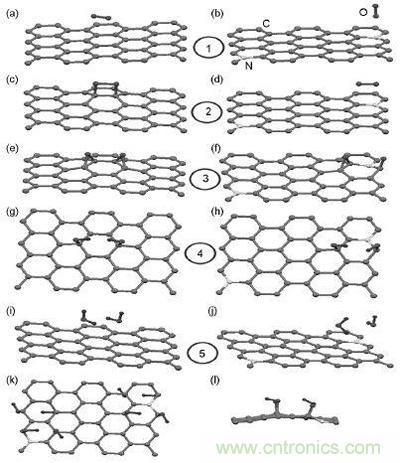
圖8.ORR在(左)完整石墨烯和(右)N石墨烯上的反應過程
科學家使用團簇結構的石墨烯模型研究了含N石墨烯在酸性環(huán)境中對O2的催化機理。計算表明,OOH吸附在靠近吡啶結構N的C原子上,其中一個O與C原子相互作用,并且該C原子從石墨烯平面伸出。對于吡咯N,OOH同樣會吸附在靠近N 的C原子上。當在OOH上進一步增加H后,吡啶N和吡咯N石墨烯上都會形成不穩(wěn)定的HOOH,O—O鍵長增加,容易變成兩個OH,所以在N石墨烯上的ORR是四電子過程。同時,作者提出自旋密度和電荷密度是決定催化效果的關鍵因素。盡管有的C電荷密度非常高,但是OOH更容易吸附在具有高自旋密度的C原子上。與電荷密度相比,自旋密度更能決定催化活性位,只有當自旋密度非常小時電荷密度才起作用。圖9給出了所計算的摻N石墨烯上電荷密度和自旋密度分布。
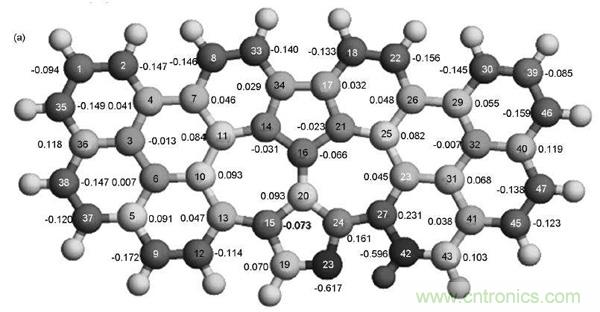
圖9.N摻雜石墨烯的(a)原子電荷密度和(b)自旋密度
Li-空氣電池負極為Li,正極的空氣電極通常為多孔炭,具有非常高的能量密度。外部的O2進入空氣電極并吸附在多孔炭的表面,隨后O2分解并與負極氧化得到的Li離子發(fā)生反應??茖W家使用周期結構模型計算了Li-空氣電池正極O2在N石墨烯表面的催化分解過程。O2分子靠近離石墨烯時,一個O原子位于N最鄰近的C原子上面并向石墨烯平面傾斜,另外一個O位于C5N環(huán)的中心,O2不再平行,O—O鍵變弱。
除了在ORR反應中的催化作用,在O2析出反應中摻雜石墨烯也具有明顯的電化學活性。理論計算表明,B摻雜的石墨烯由于缺電子,可以比完整石墨烯較強低吸附Li2O2,進而在較低能壘下活化Li—O鍵并將O2-氧化成O2。由于B摻雜的石墨烯可以在很大程度上降低決速步驟的能壘,可以有效提高鋰空電池的電流密度。